
用上脐带血,世界首位治愈艾滋病的女性出现?
在全球范围内,有近 3800 万人感染了 HIV,其中约 73% 的人正在接受治疗。抗逆转录病毒药物可以控制 HIV,但治愈艾滋病是长达数十年的难题。
在没有任何治疗手段介入的情况下,患者的免疫系统将逐渐被 HIV 摧毁,直至丧失几乎所有免疫能力,感染各种疾病或患上恶性肿瘤。

▲ 图片来自:unaids
2 月 15 日,纽约时报报道,一名在纽约威尔康奈尔医学中心接受治疗的中老年混血女性,可能是世界上第三位治愈艾滋病的人,以及第一位治愈艾滋病的女性。
研究团队将其看做一项科学突破,首先是因为她的性别和种族背景;其次是因为创新的治疗方法。

▲ 图片来自:nytimes
此前两位患者都是通过骨髓移植治愈艾滋病的男性,即「柏林病人」Timothy Ray Brown 和「伦敦病人」Adam Castillejo,前者患有急性髓性白血病,后者患有霍奇金淋巴瘤。

▲ Adam Castillejo. 图片来自:nytimes
然而,骨髓移植是一项风险和条件极高的手术,它用另一个人的免疫系统代替患者的免疫系统,治疗癌症的同时治愈艾滋病,对于大多数艾滋病患者来说并不现实。
原因在于,骨髓移植的供体,必须和患者有足够匹配的人类白细胞抗原,并携带一种阻止 HIV 感染的基因突变。这种基因突变发生率在 1% 左右,目前仅在约 2 万名供体中发现,其中大多数是北欧血统。
也就是说,缺乏相似血统的患者找到合适供体的机会特别低。
就算排除万难做完手术,也会被「移植物抗宿主病」等严重的副作用缠身。柏林病人在移植后差点去世,此后他活了没有再感染 HIV 的 12 年,最终死于复发性白血病。

▲ Timothy Ray Brown. 图片来自:Getty Images
让我们再说回开头这位混血女性的故事。因为治疗地点,她被称为「纽约病人」。她的成功案例,为患有血液恶性肿瘤的艾滋病患者,带来了副作用更小的治愈可能。
2013 年 6 月,纽约病人被诊断出感染了 HIV,并服用抗逆转录病毒药物控制病毒水平;2017 年 3 月,她患上急性髓细胞性白血病。
2017 年 8 月,这位女性接受了和脐带血有关的新移植方法。脐带血是指分娩后残留在胎盘和脐带中的血液,它包含各种类型的干细胞和祖细胞。
脐带血同样需要匹配人类白细胞抗原,并带有阻止 HIV 感染的基因突变。
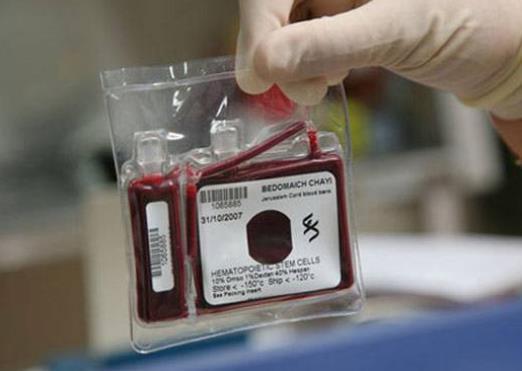
▲ 脐带血. 图片来自:央视网
但与骨髓移植中使用的成体干细胞相比,脐带血的适应性更强,不需要与受体密切匹配,引起的并发症也更少。此外,与骨髓登记处不同,脐带血资源库更容易大量筛查是否存在所需的基因突变。
纽约病人接受的脐带血,仅与她的人类白细胞抗原「部分匹配」。
与此同时,她还获得了来自近亲的造血干细胞,也和她的人类白细胞抗原「部分匹配」。这些造血干细胞在移植期间为身体提供了暂时的免疫防御,直到脐带血细胞占主导地位,从而大大降低移植的危险性。

▲ 图片来自:unaids
脐带血和造血干细胞都只是部分匹配,但两者的组合造就了最终的成功,其中的原因尚未完全清楚。研究人员猜测,脐带血可能为移植带来了额外的好处。
纽约病人在移植后第 17 天出院,未出现移植物抗宿主病;在移植后的 37 个月,她停用了抗逆转录病毒药物;再过 14 个月,患者没有任何感染 HIV 的迹象。
然而,并非所有人都同意「治愈」这个结论。加州大学洛杉矶分校儿科传染病专家 Yvonne Bryson 选择用「缓解」一词替代。如果在几年之后一如往常,或许说明纽约病人已治愈。

▲ 研究团队. 图片来自:Benjamin Ryan/nbcnews
更重要的是,新疗法适用的人群仍然有限,特指那些患有血液恶性肿瘤的艾滋病患者。而且,就算没有传统骨髓移植的破坏性大,它依然是一种危险的干细胞移植方法。
在接受 NBC 采访时,约翰霍普金斯大学医学院儿科传染病专家 Deborah Persaud 博士说道:
虽然我们对可能治愈艾滋病的新病例倍感兴奋,但干细胞治疗方法只能适用于一小部分人,对于数百万 HIV 感染者来说仍然不是一个可行的策略,比如那些没有潜在致命癌症的患者。
无论如何,「艾滋病治愈」这座大山终于又挪动了一点。威尔康奈尔医学中心移植服务主任 Koen van Besien 博士指出:
我们估计美国每年大约有 50 名患者可以从这种手术中受益。使用部分匹配的脐带血移植物,大大增加了为此类患者找到合适供体的可能性。

▲ 自愈患者. 图片来自:acpjournals
纽约病人被称为第三个「治愈」案例,此前也存在一些未经干细胞移植等治疗的「自愈」患者,例如「旧金山病人」和「埃斯佩兰萨病人」,她们自身的免疫系统治愈了 HIV,被称为「精英控制者」,研究人员正在研究背后的免疫机制。

















